- 52 件中「NDA」が過半数を占める…FDA の承認フローは「合成医薬品」が中心
- 痛み、中枢神経系、代謝性疾患の進歩…長期処方を対象としたパイプラインの拡大
- 大ヒット拡張、新機構…「キイトルーダ SC」と「ゼルナベックス」に注目
- 「BLA」は主にワクチンと遺伝子治療に焦点を当てています…「Penmenbi」と「Vimcuña」の承認
[バイオ記者ソン・ジェジュン] 米国食品医薬品局(FDA)は今年、合計52種類のオンラインカジノアプリを承認し、痛み、神経系、代謝性疾患などの慢性疾患を中心とした新たな治療選択肢が次々と商業化の閾値を超えている。年末のFDAオンラインカジノアプリ承認状況を見ると、治療分野と技術軸の両方で変化の傾向がはっきりと表れている。特に、Vertex Pharmaceuticals(バーテックス)の非麻薬性鎮痛剤「Journavx(自家製トリジン)」は、既存のオピオイド鎮痛剤の限界を補完できる新たな代替薬として注目を集めており、今年FDAが承認したオンラインカジノアプリの中で最も注目を集めた薬剤と考えられている。中毒や依存のリスクを軽減するメカニズムを活用することで、慢性疼痛の治療環境に変化をもたらすことができるかどうかに関心が高まっています。
国内の製薬およびバイオ産業に関連したオンラインカジノアプリの出現も目立っています。売上高世界No1のMSD社(米国メルク社)のがん免疫治療薬「キイトルーダ」の皮下注(SC)製剤として承認された「キイトルーダQLEX(成分:ペムブロリズマブ/ベラヒアルロニダーゼアルファ、以下キイトルーダSC)」は、その投与の容易性と製剤変換技術を提供した国内企業が世界的な大ヒット商品になる可能性があると話題になっているバイオテクノロジー企業 Alteogen にも注目が集まりました。
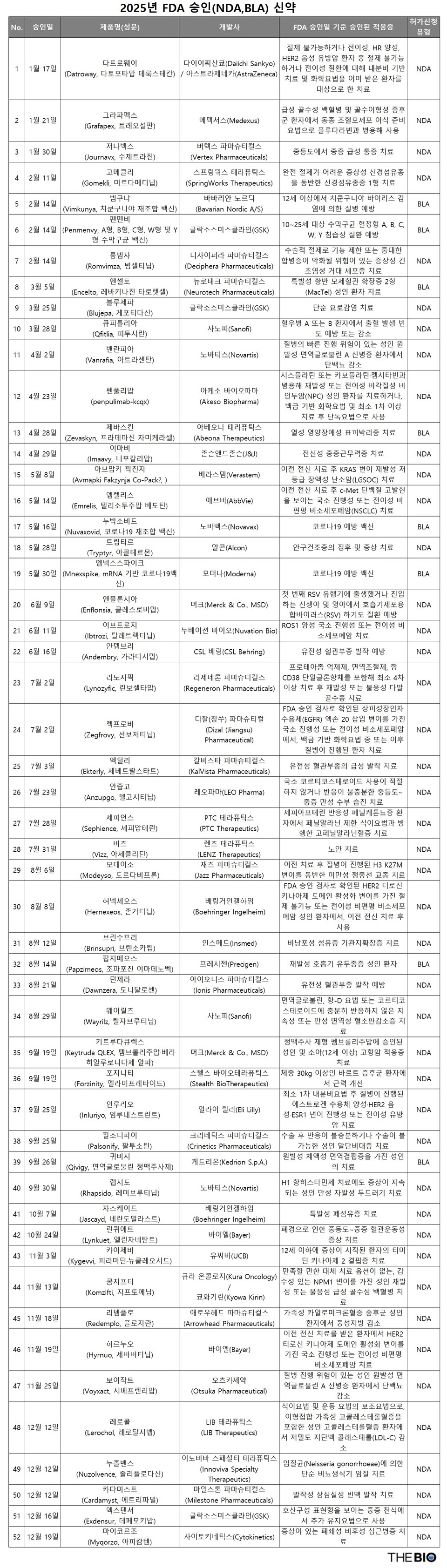
29日の<TheBio>の分析の結果、今年FDAが承認したオンラインカジノアプリのうち、合成オンラインカジノアプリ(NDA)が大半を占め、ワクチンや遺伝子治療などの生物学的オンラインカジノアプリ(BLA)は特定の治療分野に集中する傾向があった。この集計には、今年1月から12月までに新たに承認されたNDAおよび新BLA品目のみが含まれており、適応追加追加承認(sNDA・sBLA)や診断薬などの非治療薬は含まれていない。
◇52件中NDAが過半数…FDAの承認フローは合成医薬品中心
今年承認された52のオンラインカジノアプリのうち、NDAが半分以上を占め、合成医薬品を中心としたFDAの承認傾向が続いている。痛み、神経系、代謝性疾患、心血管疾患など、患者数が多い適応症を対象とした薬剤が大半を占め、臨床効果と安全性が明確な候補物質は比較的早く承認されました。
適応症別では、「抗がん剤」が最大の割合を占めた。今年FDAが承認した52のオンラインカジノアプリのうち、がんの適応症として承認されたのは約14薬で、全体の3分の1近くを占めた。今年の FDA の承認フローのもう 1 つの特徴は、オンラインカジノアプリの承認が患者数の多い適応症、特にがんに集中していることです。
◇ 痛み、中枢神経系、代謝性疾患の進歩…長期処方に向けたパイプライン拡大
治療分野別では、疼痛、中枢神経系(CNS)、代謝性疾患に関連するオンラインカジノアプリの割合が著しく拡大しています。慢性疼痛や神経疾患、肥満、糖尿病など長期にわたる治療が必要な疾患では、新たなメカニズムをもつ薬が次々に承認されており、既存の治療法を補完したり置き換えたりする可能性が示唆されています。この傾向は、短期的な販売ではなく長期的な処方と市場拡大に重点を置く世界的な製薬会社の戦略的変化とも一致しています。
◇大ヒット拡大と新たな仕組みの登場…キイトルーダSCとゼルナベックスに注目
特に、非麻薬性鎮痛薬として差別化されたメカニズムを誇るバーテックス社の「ゼルナベックス」は、既存のオピオイド鎮痛薬の限界を補完できる代替薬として評価されており、今年承認されたオンラインカジノアプリの中でも最も象徴的な事例の一つと考えられている。中毒や依存症のリスクを低下させながら、大きな鎮痛効果があることが証明されているため、将来の市場拡大の可能性についても話されています。
◇BLAはワクチンと遺伝子治療に注力…ペンメンビ氏とヴィムクニャ氏が承認
BLA が承認した品目は、「ワクチン」と「遺伝子治療製品」に重点が置かれていました。代表的な例としては、髄膜炎菌ワクチン「PENMENVY」やチクングニア熱ワクチン「VIMKUNYA」などがあります。感染症対応能力の強化は世界的な公衆衛生のニーズと一致しており、予防目的の生物製剤が依然として FDA の承認戦略の重要な分野であることを示しています。
さらに、希少疾患を対象とした遺伝子治療もBLAの承認リストに含まれました。アベオナ・セラピューティクス社の発熱性ジストロフィー表皮溶解療法剤「ゼバスキン」(成分:プラデマジン・ジン・ザミケラセル)やオーチャード・セラピューティクス社のウィスコット・アルドリッチ症候群治療剤「ワスカイラ(成分:エツベティジジェン・オートテムセル)」は、治療法が限られている希少疾患でも承認されている。遺伝子治療の承認の流れは続いた。
