- タンパク尿と eGFR に基づく規制システムの確立「Tarpeyo」、「Filspari」、「Voyzact」が新薬への移行を主導
- 日本では、レナリスが「スパルセンタン」の臨床試験を完了…来年のNDA提出によりアジアでの商業化が本格的に始まる
- ノバルティスとベラが後発として競争に参加ボッチェ/BAFF/APRILをベースにした次世代ラインナップの出現
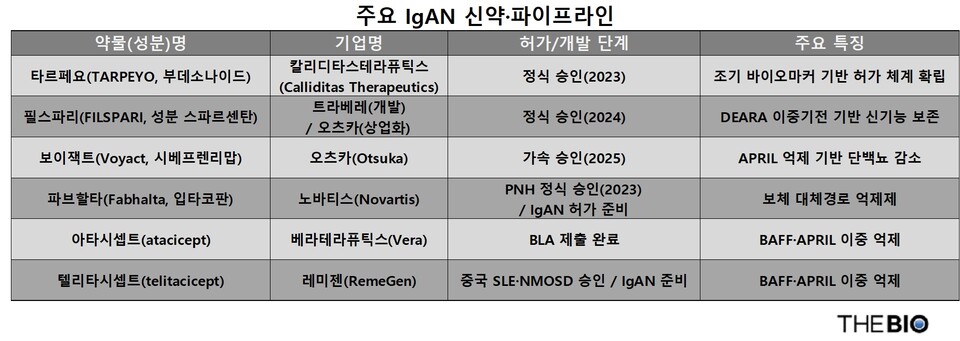
[ザ・バイオ ソン・ジェジュン記者] 「免疫グロブリンA腎症(オンラインカジノ日本)」治療市場が本格的に「新薬競争の時代」に突入している。多国籍製薬会社である大塚製薬を含む世界的な製薬会社は、腎機能の悪化を遅らせ、疾患メカニズムを制御することを目的とした新薬に関するデータを確保し続けているため、オンラインカジノ日本治療は、RAS阻害を中心とした既存の支持療法から、メカニズムに基づいた治療へと急速に移行しつつある。
最近、米国食品医薬品局 (FDA) が主要な オンラインカジノ日本 新薬の承認または確認データを次々と承認し、規制環境が再編されています。 FDAは、タンパク尿の早期抑制と糸球体濾過率(eGFR)の傾きの緩和を重要な判断基準として明確に提示しており、それに応じて開発者の新薬戦略も加速しているようだ。 オンラインカジノ日本は若年者から発症し、10~20年以内に半数が腎不全に進行する難病ですが、既存の治療法だけで十分にコントロールすることは困難です。
◇オンラインカジノ日本治療のパラダイムシフト…タルペヨ、スパセンタン、ボイザクトの3種が新薬時代をリードする
30820_31116
31125_31513
米国のTravere Therapeutics社(以下、Travere社)が開発し、大塚製薬が世界的に商業化した経口(成分)デュアル受容体拮抗薬であるFILSPARI(成分スパルセンタン)は、第3相臨床試験(PROTECT)の確認データに基づき、昨年、迅速承認から正式承認に移行した。スパルセンタンは、疾患の進行に影響を与えるエンドセリン A-アンジオテンシン II 経路を同時にブロックする DEARA 二重機構により、既存の実薬対照である「イルベサルタン」と比較して eGFR の低下速度を大幅に遅らせる有効性を実証したことにより、新しい標準治療候補として浮上しました。
さらに、大塚製薬の抗APRIL抗体「Voyact(成分シベプレンリマブ)」は、先月25日にFDAから早期承認を取得し、オンラインカジノ日本治療の選択肢の幅が大幅に広がりました。 Voizactは、国際共同第3相臨床試験(VISIONARY)の中間結果で9ヵ月後のタンパク尿の51%減少を記録し、FDAはこの薬剤を成人オンラインカジノ日本患者のタンパク尿を減らす治療法として承認した。既存治療法の表示によく含まれていたハイリスクや急速な進行の条件が省略され、ベースライン時の蛋白尿基準(15g/日以上)も明記されていないため、実際の処方対象者はさらに広いのではないかとの評価となっている。ただし、早期承認であるため、最終的な承認は2026年に公開予定のeGFR確認データに依存します。
◇レナリスは日本でスパルセンタン臨床試験を実施…2026年にNDA申請予定
日本では、スパルセンタンの開発と承認はトラヴェリーナ大塚ではなく、多国籍製薬会社ロシュの子会社である中外製薬の100%子会社であるレナリス・ファーマ(レナリス)が担当している。レナリスは日本人 オンラインカジノ日本 患者を対象にブリッジング研究を実施し、36 週間でのタンパク尿の 5854% 減少など、世界的な研究と一致する結果を確認しました。
このデータに基づいて、レナリスは2026年に日本の薬事当局にスパルセンタンの新薬申請(NDA)を提出することを正式に決定した。日本はオンラインカジノ日本治療の選択肢が非常に限られた市場であるため、スパルセンタンの承認の可能性に期待が高まっている。
◇ノバルティス・ベラ、補体ベースの次世代治療法競争・BAFF・APRIL
オンラインカジノ日本後発パイプラインの中で、多国籍製薬会社ノバルティス社の補体代替経路阻害剤である「ファバルタ(成分イプタコパン)」は、商業化に最も近い候補として評価されている。ファバルタはすでに2023年12月に発作性夜間ヘモグロビン尿症(PNH)の治療薬としてFDAから正式に承認されており、経口単剤療法として商業基盤を確保している。
オンラインカジノ日本 分野では、国際共同第 3 相臨床試験 (APPLAUSE-オンラインカジノ日本) により、eGFR の低下速度を 2 年間大幅に遅らせて腎機能を温存する効果を証明し、主要な競争軸としての地位を確立しつつあります。 このデータに基づいて、ノバルティスは 2026 年に適応症として オンラインカジノ日本 の正式承認申請を FDA に提出する予定です。
米国ベラ・セラピューティクス社(以下ベラ社)のアタシセプトも、後発企業の中で最も早く実用化段階に近い候補として評価されている。本剤は、BAFFとAPRILを同時に阻害する機序に基づいて実施された第3相臨床試験(ORIGIN)の中間解析において、プラセボと比較してタンパク尿46%減少、42%改善という有意な有効性が確認されました。 Vera はこれらの結果に基づいて生物製剤ライセンス申請 (BLA) をすでに提出しており、アタシセプトは BAFF/APRIL 阻害剤の中で承認の可能性が検討される最初の候補として評価されています。
33635_33947
