- 23 年間で FDA 新薬「二桁」時代が目前に迫っている…HLB・HK イノエン承認の課題
- ABL Bio・Ari Bio グローバル臨床データ コンペティション
- アルテオジェン「ALT-B4」とユーハンコーポレーション「ラゼルチニブ」のロイヤルティが可視化…「商品化利益」セクションに入る
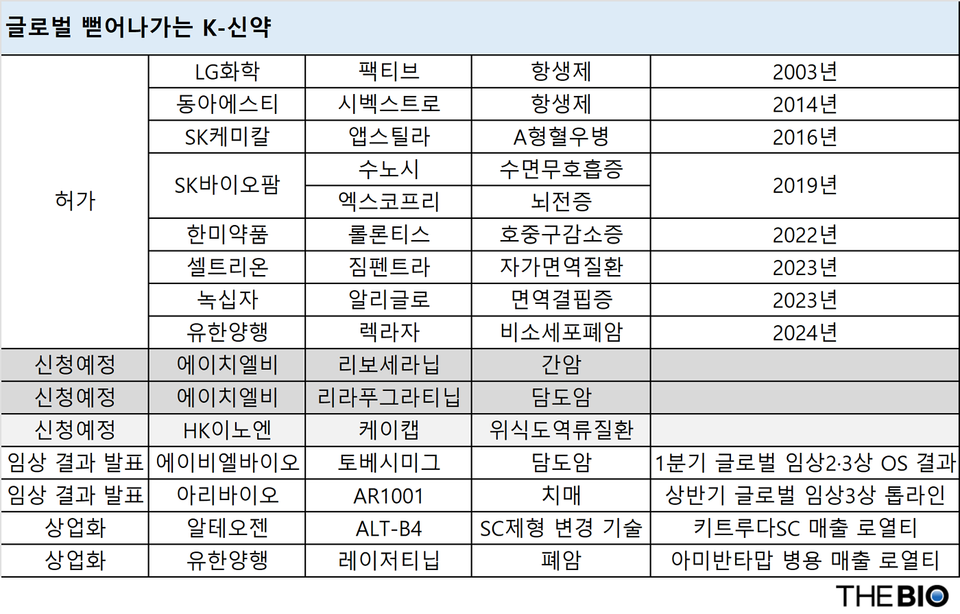
[バイオ記者チ・ヨンジュン] 国内製薬企業とバイオ企業が今年もオンラインカジノポーカー舞台への挑戦を続けている。長年にわたって懸命に取り組んできた国産新薬のパイプラインは、米国食品医薬品局(FDA)の基準を通過するための課題を予感させている。特に、開発中の新薬候補のオンラインカジノポーカー臨床トップラインが発表されるだけでなく、すでに実用化された新薬に対する多額のロイヤルティ収入も本格化すると予想されます。
リラフグラチニブは、線維芽細胞増殖因子受容体 (FGFR) の変異と再配列を標的とする精密医療ベースの抗がん剤候補であり、胆管がんなどの固形がんを対象に開発されています。リラフグラチニブは米国で「希少疾病用医薬品(ODD)」に指定されており、早期の製品承認の基礎を築きました。
HK イノエンの胃食道逆流症の新薬「K-Cap」も米国市場に参入する予定です。米国のパートナーである Sevela の子会社である Braintree は、第 3 相臨床試験を無事に完了しており、近い将来 FDA の製品承認を申請する予定です。 K-Capが国内市場に続いて米国市場にも定着すれば、オンラインカジノポーカー的な大ヒット作に挑戦できるものと予想される。
FDA の承認申請段階に入った候補物質に加え、臨床結果の発表を間近に控えた次世代パイプラインの勢いも強い。 ABL Bioのパートナー企業であるCompass Therapeutics(以下、Compass)は、開発中の「Tobesimig(開発コード名ABL001)」の胆道がん第2相および第3相臨床試験の全生存期間(OS)データを今年第1四半期に発表する予定である。有意義な結果が得られれば、FDAに新薬承認申請(BLA)を申請する予定です。
Tobesimig は、「DLL4」と「VEGF-A」を同時にブロックする二重抗体であり、血管新生を阻害する作用機序が異なる VEGF と DLL4 を同時に阻害することで、VEGF 耐性を克服し、強力な抗がん活性を発揮するように設計されています。昨年、コンパスは胆道がんを対象としたトベシミグの第2相および第3相臨床試験の追跡調査を続けていたが、患者の死亡率が低下し続けたため、OSデータの発表のタイミングが今年の第1四半期末に調整された。業界は、スケジュールの調整は患者の生存期間の延長の結果であるため、薬の有効性の持続可能性を証明する強力な前向きのシグナルであると解釈しています。
アリビオは、経口(食用)アルツハイマー病治療薬候補である「AR1001(開発コード名)」の国際第3相臨床試験のトップライン結果を今年第2四半期中に発表する予定です。 AR1001の主成分は「ミロデナフィル」で、PDE5阻害剤クラスに属する経口薬です。 PDE5阻害剤は、既存の勃起不全治療薬である「バイアグラ(成分シルデナフィル)」としてよく知られています。 Aribio はまた、FDA の「迅速審査システム」を通じて年内に製品承認される予定です。
さらに、今年は、Alteogen と Yuhan Corporation が主導するオンラインカジノポーカー的な商業化からのロイヤルティが完全に目に見える最初の年と考えられています。 アルテオジェン社のヒトヒアルロニダーゼ「ALT-B4」技術を応用した多国籍製薬会社MSD(米メルク)の免疫療法薬「キイトルーダ」の皮下注射(SC)製剤が昨年、FDAと欧州医薬品庁(EMA)から相次いで製品承認を取得した。米国と欧州では、それぞれ「キイトルーダ キュレックス」、「キイトルーダ SC」という製品名で販売されています。 ALT-B4 は、静脈内 (IV) 製剤のバイオ医薬品を皮下製剤に変換するプラットフォーム技術です。
したがって、キイトルーダ製剤への切り替えにより、アルテオジェンは今年から本格的に販売ロイヤルティを発生し始めることが予想されます。 MSDはキイトルーダの全処方箋の40%をSC製剤に転換することを推進しており、業界はアルテオジェンの年間ロイヤルティ収入が数兆ドルに達すると予測している。これは国産バイオプラットフォーム技術が生み出す利益の頂点を示す一例と考えられる。
ユハンコーポレーションの上皮成長因子受容体(EGFR)変異非小細胞肺がん(NSCLC)の新薬「ラゼルチニブ(米国名:ラズクルーズ、韓国名:レクラザ)」もオンラインカジノポーカー的大ヒット目前だ。パートナー企業のジョンソン・エンド・ジョンソン(J&J)を通じて米国に参入した「ラセルチニブとアミバンタマブ(製品名リブバント)」の併用療法は、最近米国国家総合がんネットワーク(NCCN)のガイドラインで非小細胞肺がんの第一選択治療の「優先治療法」に挙げられ、市場拡大の基礎を築いた。
特に、米国におけるアミバンタマブの皮下製剤の承認により、投与の利便性が向上し、ラゼルチニブの市場シェアは急激に上昇すると予想されます。 経口投与のラゼルチニブと皮下製剤のアミバンタマブの併用療法により、治療の利便性が向上し、処方拡大に有利となることが期待されるためである。したがって、ユーハンコーポレーションは、ラゼルチニブのオンラインカジノポーカー的な販売により、安定したロイヤルティ収入を確保することが期待される。国産新薬が技術輸出を経て、オンラインカジノポーカー的な商業化段階で成果を上げる初の事例となる見込み》
